Modifikasi Gugus Amin Dan Imin
- Dapatkan link
- X
- Aplikasi Lainnya
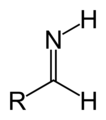
Imina atau imino adalah gugus fungsi atau senyawa kimia yang mengandung ikatan rangkap karbon–nitrogen. Atom nitrogen dapat melekat pada hidrogen (H) atau gugus organik (R). Jika gugus ini bukan atom hidrogen, maka senyawa tersebut kadang-kadang dapat dirujuk sebagai basa Schiff.[1] Atom larbon atom memiliki tambahan dua ikatan tunggal
Imina ( / ɪ ˈ m ː n / atau / ˈ ɪ m ɪ n / ) adalah gugus fungsi atau senyawa kimia yang mengandung ikatan rangkap karbon - nitrogen . Atom nitrogen dapat dilekatkan ke hidrogen (H) atau grup organik (R). Jika kelompok inibukan atom hidrogen, maka senyawa tersebut kadang-kadang dapat disebut sebagai pangkalan Schiff . [1] Atom karbon memiliki dua ikatan tunggal tambahan. [2] [3] [4] Istilah "imine" diciptakan pada tahun 1883 oleh kimiawan Jerman Albert Ladenburg . [5]
Nomenklatur dan klasifikasi
Biasanya imina mengacu pada senyawa dengan konektivitas R 2 C = NR, seperti yang dibahas di bawah ini. Dalam literatur yang lebih tua, imina mengacu pada analog aza dari epoksida. Dengan demikian, etilenimin adalah spesies cincin beranggota tiga C2H4 NH. [6]
Imina terkait dengan keton dan aldehid dengan penggantian oksigen dengan kelompok NR. Ketika R = H, senyawa tersebut adalah imina primer, ketika R adalah hidrokarbil , senyawa tersebut adalah imina sekunder. Imina menunjukkan reaktivitas yang beragam dan biasanya ditemui di seluruh kimia. [4] Ketika R 3 adalah OH, imine disebut oksime , dan ketika R 3 adalah NH 2 imina disebut hidrazon .
Imina primer di mana C melekat pada hidrokarbil dan H disebut aldimine primer ; imina sekunder dengan kelompok seperti ini disebut aldimine sekunder . [7] Imina primer di mana C melekat pada dua hidrokarbil disebut ketimine primer ; imina sekunder dengan kelompok seperti ini disebut ketimin sekunder . [8]
- Aldimine primer
- Aziridine dan turunannya kadang-kadang disebut sebagai imina.
Salah satu cara menamai aldimines adalah dengan mengambil nama radikal, hapus "e" akhir, dan tambahkan "-imine", misalnya ethanimine . Lihat artikel aldimine untuk konvensi penamaan lainnya.Secara bergantian, sebuah imina dinamakan sebagai turunan dari karbonil, menambahkan kata "imina" ke nama senyawa karbonil yang gugus oksonya digantikan oleh kelompok imino , misalnya imon sydnone dan imina aseton (zat antara dalam sintesis). acetone azine ).
N-Sulfinyl imines adalah kelas khusus imina yang memiliki gugus sulfinil yang terikat pada atom nitrogen.
Sintesis imina
Imina biasanya disiapkan oleh kondensasi amina primer dan aldehida dan keton kurang umum:
- RNH 2 + R′C (O) R ′ ′ → RN = C (R ′) (R ′ ′) + H 2 O
Dalam hal mekanisme, reaksi tersebut dilanjutkan melalui penambahan nukleofilik memberikan hemiaminal -C (OH) (NHR) - menengah, diikuti dengan eliminasi air untuk menghasilkan imina. (lihat alkylimino-de-oxo-bisubstitution untuk mekanisme terperinci) Kesetimbangan dalam reaksi ini biasanya mendukung senyawa karbonil dan amina, sehingga distilasi azeotropik atau penggunaan agen dehidrasi, seperti saringan molekuler atau magnesium sulfat , diperlukan untuk mendorong reaksi yang mendukung pembentukan imina. Dalam beberapa tahun terakhir, beberapa reagen seperti Tris (2,2,2-trifluoroethyl) borat [B (OCH 2 CF 3 ) 3 ], [9] pyrrolidine [10] atau titanium ethoxide [Ti (OEt) 4 ] [11] telah terbukti mengkatalisis pembentukan imina.
Lebih banyak metode khusus
Beberapa metode lain ada untuk sintesis imina.
- Reaksi dari azida organik dengan logam carbenoid (diproduksi dari senyawa diazocarbonyl). [12]
- Kondensasi asam karbon dengan senyawa nitroso .
- Penataan ulang trityl N-haloamines dalam penataan ulang Stieglitz .
- Dehidrasi hemiaminal . [13]
- Dengan reaksi alkena dengan asam hidrazoat dalam reaksi Schmidt .
- Dengan reaksi asam nitril, asam klorida, dan aren dalam reaksi Hoesch .
- Sintesis multikomponen 3- tiazolina dalam reaksi Asinger .
- Ketimin primer dapat disintesis melalui reaksi Grignard dengan nitril . [14] [15]
Reaksi imina
Hexafluoroacetone imine adalah ketimine primer yang tidak biasa yang stabil.
Reaksi yang paling penting dari imina adalah hidrolisis mereka ke senyawa amina dan karbonil yang sesuai. Jika tidak, gugus fungsi ini berpartisipasi dalam banyak reaksi lain, banyak yang analog dengan reaksi aldehida dan keton.
- Imina berkurang dalam aminasi reduktif .
- Imina bereaksi dengan amina ke aminal , lihat misalnya sintesis cucurbituril .
- Sebuah imina bereaksi dengan diena dalam reaksi Aza Diels-Alder ke tetrahidropiridin.
- Imina dapat dioksidasi dengan asam meta-kloroperoksibenzoat (mCPBA) untuk memberikan oksaziridin
- Sebuah imina aromatik bereaksi dengan enol eter ke quinoline dalam reaksi Povarov .
- A tosylimine bereaksi dengan senyawa karbonil α, β-unsaturated ke amina alilik pada reaksi Aza-Baylis-Hillman .
- Imina adalah perantara dalam alkilasi amina dengan asam format dalam reaksi Eschweiler-Clarke .
- Penataan ulang dalam kimia karbohidrat yang melibatkan imina adalah penataan ulang Amadori .
- Reaksi transfer metilena dari imina oleh sulfonium ylide tidak stabil dapat memberikan sistem aziridine .
- Imina bereaksi, secara termal, dengan ketena dalam sikdisi siklik [2 + 2] untuk membentuk β-laktam dalam sintesis Staudinger .
- Sebuah imina dapat bereaksi dengan dialkilfosfit dalam reaksi Pudovik dan reaksiKabachnik-Fields
Reaksi asam-basa
Agak seperti induk amina, imina sedikit bersifat basa dan dapat berefleksi secara reversibel untuk menghasilkan garam iminium. Turunan iminium sangat rentan terhadap reduksi ke amina menggunakan transfer hidrogenasi atau dengan aksi stoikiometrik natrium cyanoborohidrida .Karena imina yang berasal dari keton yang tidak simetris bersifat prokiral , reduksi mereka adalah metode yang berguna untuk sintesis amina kiral.
Sebagai ligan
Imina adalah ligan umum dalam kimia koordinasi . Kondensasi salicylaldehyde dan ethylenediaminememberi keluarga agen chelating yang mengandung imine seperti salen .
Pengurangan imina
Artikel utama: Hidrogenasi ikatan ganda karbon-nitrogen
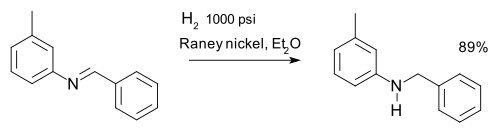
Imina dapat direduksi menjadi amina melalui hidrogenasi misalnya dalam sintesis m -tolylbenzylamine: [16]
Zat pereduksi lain adalah lithium aluminium hidrida dan natrium borohidrida . [17]
Asymmetric imine reduction pertama dilaporkan pada tahun 1973 oleh Kagan menggunakan Ph (Me) C = NBn dan PhSiH 2 dalam hidrosililasi dengan ligan kiral Katalis DIOP dan rhodium (RhCl (CH 2 CH 2 ) 2 ) 2 . [18] Banyak sistem telah diselidiki. [19] [20]
Modifikasi kimia dari protein tiol dengan reduksi dan alkilasi adalah umum dalam persiapan sampel proteomik untuk analisis dengan spektrometri massa (MS). Modifikasi pada kelompok fungsional lainnya kurang mendapat perhatian pada proteomik berbasis-MS. Modifikasi amina (Lys, N-termini) oleh dimetilasi reduktif atau dengan asilasi (misalnya pelabelan iTRAQ) baru-baru ini mendapatkan popularitas dalam pendekatan berbasis peptida (MS dari bawah). Modifikasi pada kelompok asam (Asp, Glu, C-termini) telah dieksplorasi sangat minim. Di sini, kami menggambarkan strategi pelabelan berurutan yang memungkinkan modifikasi lengkap tiol, amina, dan asam pada peptida atau protein utuh kecil. Metode ini termasuk (1 ) reduksi dan alkilasi tiol, ( 2 ) reduksi dimetilasi amina, dan ( 3 ) penengahan asam dengan beberapa amina. Skema modifikasi kimia ini menawarkan beberapa pilihan baik untuk penggabungan isotop stabil untuk kuantifikasi relatif dan untuk meningkatkan peptida atau protein sebagai analit MS.
Modifikasi Grup Amino
Modifikasi gugus amino melibatkan penambahan gugus fungsi pada ujung N dari asam amino .
Protein setelah terjemahannya mengalami modifikasi kimia yang disebut Post Translational Modification . Modifikasi ini dapat mengubah fungsi protein ketika melekat pada kelompok fungsional biokimia seperti asetat dengan mengubah sifat kimia dari asam amino atau dengan perubahan struktural seperti lipat, distribusi konformasi, stabilitas, aktivitas dll.
Jenis Modifikasi Grup Amino
Asetilasi
Asetalisasi adalah proses asilasi (pengantar gugus asil ke senyawa organik) yang melibatkan substitusi gugus asam asetat organik untuk atom hidrogen aktif pada N-terminus.
Modifikasi paling luas pada eukariota adalah Asetilasi dari kelompok protein α-amina N-terminal.Sekitar 50% protein ragi dan sekitar 90% protein pada manusia dimodifikasi oleh mekanisme ini.Pola modifikasi dilestarikan sepanjang evolusi. Meskipun itu adalah modifikasi umum, tidak banyak informasi yang tersedia untuk tentang fungsi biologis dari asetilasi N-α-terminal. N-α-acetyltransferase (NATs) adalah enzim yang bertanggung jawab untuk Asetilasi. NAT milik keluarga GNAT, yang terletak di bawah superfamili acetyltransferases . [1]
Asetilasi dan deasetilasi terjadi pada residu lisin di ekor N-terminal di asetilasi dan deasetilasi histone . Reaksi-reaksi ini terjadi di hadapan enzim histone acetyltransferase (HAT) atau histone deacetylase (HDAC).
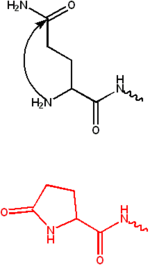
Formasi Pyroglutamate
Pyroglutamate terbentuk melalui siklisasi (pembentukan cincin dalam senyawa kimia) glutamin .Ini biasanya diamati pada antibodi yang mengandung residu glutamat atau glutamin pada N-termini. Gugus amino dan glutamat atau glutamin mengembun membentuk cincin lima anggota yang disebut Pyroglutamate. Residu ini membuat protein lebih tahan terhadap aminopeptidasedan memiliki banyak peran fungsional. [2]
Ia mempertahankan integritas struktural pada N-terminal α-helix dan menyediakan lingkungan yang tepat untuk ionisasi residu Histidin untuk katalisis dan sitotoksisitas terhadap sel HeLa .
Myristoylation
N-myristoylation juga merupakan proses asilasi yang ditemukan khusus untuk gliserin asam amino N-terminal dalam protein di mana kelompok myristoy (berasal dari asam miristat) secara kovalen dilampirkan melalui ikatan amida dengan gugus alpha-amino N-terminal Glycine. Myristoylation memainkan peran penting dalam pensinyalan seluler sekunder, dalam infektivitas retrovirus dan onkogenesis pada Eukariota. Ini juga mempengaruhi fungsi fisiologis protein pengikat kalsium. [3]Enzim cytosolic N-myristoyltransferase (NMT) mengkatalisis Myristoylation.
Methylation
Metilasi protein adalah bentuk modifikasi pasca-translasi yang paling umum yang diamati. Mirip dengan modifikasi pasca-translasi lainnya, metilasi protein terlibat dalam mengatur interaksi protein-protein yang menghasilkan sejumlah besar efek selama peristiwa seluler utama, termasuk pengaturan transkripsi [4] [5] [6] respon stres, penuaan dan perbaikan protein [ 7] Aktivasi sel-T [8] , transportasi nuklir [9] , diferensiasi neuronal [10] , [11] fungsi saluran ion, dan pensinyalan sitokin.Protein dianggap termetilasi ketika kelompok metil ditambahkan pada satu atau lebih rantai samping nukleofilik. Metilasi pada rantai samping nitrogens dianggap sangat tidak dapat diubah sementara metilasi dari gugus karboksil berpotensi reversibel. Residu protein yang termetilasi pada nitrogen termasuk e-amin dari lisin, cincin imidazol histidin, bagian guanidino arginin, dan rantai samping amida nitrit glutamin dan asparagin.
Metilasi dalam protein meniadakan muatan negatif di atasnya dan meningkatkan hidrofobisitas protein. Metilasi pada rantai samping karboksilat menutupi muatan negatif dan menambah hidrofobik. N-Metilasi lisin tidak mengubah muatan kationik tetapi meningkatkan hidrofobik.Khususnya, dimetilasi dan trimetilasi rantai samping lisin dalam protein meningkatkan baik hidrofobik dan massa sterik dan dapat mempengaruhi interaksi protein-protein jika mereka berada dalam permukaan yang berinteraksi.
Karbamilasi
Karbamilasi terjadi ketika asam isocyanic (HCNO) bereaksi dengan residu amino terminus, seperti lisin, dari protein. Ini adalah salah satu modifikasi protein artifactual umum yang diakui untuk fokus Isoeletric . Faktor risikonya adalah urea (chaotrope) yang ada dalam larutan dan berada dalam kesetimbangan dengan amonium sianat . Asam isosianat adalah bentuk sianat yang bereaksi dengan gugus amino protein. Untuk karbamilasi terjadi gugus asam amino protein seperti lisin, rantai samping arginin harus terdeprotonasi yang biasanya terjadi pada pH basa.Karbamilasi terjadi ketika protein dibiarkan pada suhu kamar dalam larutan urea dan di mana asam isosianat dapat dengan bebas bereaksi dengan protein.
Karbamilasi oleh asam isosianat negatif untuk langkah selanjutnya dari karakterisasi protein karena asam isosianat bereaksi dengan ujung amino protein memblokir peptida atau protein ke sekuens N-terminal. Asam isosianat menyerang rantai samping residu lisin dan arginin yang membuat protein tidak cocok untuk banyak pencernaan enzim. Bahkan jika karbamilasi tidak mencegah digest enzimatik, seringkali akan membingungkan hasil dari eksperimen spektroskopi massa dengan peptida yang memiliki waktu retensi dan massa yang tidak terduga. Karbamilasi protein in vivo diamati di beberapa negara berpenyakit. [12]
Formilasi
Formilasi adalah salah satu modifikasi posttranslational protein, di mana protein dimodifikasi oleh lampiran kelompok formil. Mekanisme yang paling umum dipelajari adalah N6-formilasi lisin yang terkait dengan histone dan protein nuklir lainnya. Modifikasi translasi post histone dan protein kromatin lainnya memainkan peran dalam fisiologi ekspresi gen . "Residu N6-formil-lisin muncul untuk mewakili modifikasi sekunder histone endogen, yang mengandung kesamaan kimia dengan lisin N6-asetilasi yang diakui sebagai penentu penting ekspresi gen pada sel mamalia." Dari penelitian itu disimpulkan bahwa modifikasi N6-formil dari lisin mengganggu fungsi sinyal asetilasi dan metilasi, yang memainkan peran dalam fisiologi stres oksidatif dan nitrosatif. [13]
Amina adalah senyawa organik dan gugus fungsi yang mengandung nitrogen basa dengan pasangan elektron bebas. Perlindungan nitrogen terus menarik banyak perhatian dalam bidang kimia, seperti peptida, nukleosida, polimer dan sintesis ligan. Tetapi, dalam beberapa tahun terakhir, sejumlah gugus pelindung nitrogen telah digunakan sebagai pembantu kiral. Dengan demikian, desain baru, lebih ringan dan metodenya lebih efektif untuk perlindungan nitrogen masih aktif dalam topik sintesis kimia.
Gugus Pelindung imida dan amida: Kelompok ftalimida telah berhasil digunakan untuk melindungi gugus amino. Pembelahan dari N-alkilftalimida (1,81) mudah dilakukan dengan hidrazin, dalam larutan panas atau dalam dingin untuk waktu yang lama untuk memberikan (1,82) dan amina. Basa katalis hidrolisis N-alkilftalimida (1.81) juga memberikan yang sesuai amina.
Modifikasi Kitosan
Adanya gugus amina (NH2) dan dan hidroksil (OH) dari kitosan menyebabkan kitosan mudah dimodifikasi secara kimia.
Gugus aktif pada kitosan
Bila dibutuhkan perubahan gugus fungsional untuk menghalangi gangguan dalam beberapa rangkaian reaksi sintesis, salah satu caranya adalah dengan menggunakan gugus pelindung. Gugus pelindung merupakan suatu turunan yang dapat dibuat dan kemudian dihilangkan. Tiga syarat-syarat yang perlu diperhatikan dalam memilih gugus pelindung adalah sebagai berikut :
1. Gugus pelindung yang digunakan harus lebih reaktif
2. Gugus pelindung yang dipakai harus dengan mudah bereaksi dengan molekul target.
3. Kondisi reaksi dalam memasukkan gugus pelindung harus stabil.
4. Dapat dimasukkan pada kondisi reaksi lunak
5. Gugus pelindung harus dapat dengan mudah dihilangkan tanpa menggangu reaksi akhir.
Reaksi penggunaan gugus pelindung pada kitosan dikarenakan kitosan memiliki 2 gugus fungsi yang kereaktifan berbeda. Gugus amino dari kitosan lebih reaktif dari pada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan, perlu dilakukan proteksi atau perlindungan terhadap gugus amino. Basa shiff dapat digunakan sebagai gugus pelindung pada reaksi O-asilasi.
Gugus amino kitosan lebih reaktif daripada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amin selama proses asilasi untuk menghasilkan O-Asil kitosan. Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff. Reaksi antara kitosan dengan anhidrida asetat menghasilkan senyawa ester yang merupakan kitosan asetat. Dalam hal ini kitosan terlebih dahulu direaksikan dengan asetaldehida membentuk aldimin untuk melindungi gugus amina. Kitosan laurat diperoleh dari reaksi transesterifikasi antara metil laurat dengan kitosan asetat. Selanjutnya dilakukan deproteksi dengan menambahkan natrium bikarbonat untuk memperoleh kitosan laurat.
Basa Schiff dapat digunakan sebagai gugus pelindung pada gugus amin (NH2), dilakukan dengan melarutkan kitosan terasetilasi dalam asam formiat 90% yang mengandung asetat anhidrida dengan asumsi protonasi akan mencegah terjadinya N-asilasi. Selanjutnya direaksikan dengan asilklorida dalam karbon triklorida dan piridin kering.
Contoh lain gugus pelindung untuk NH2 yaitu:
Gugus amino, N dari kitosan lebih reaktif dari pada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amino. Reaksi O-asilasi dapat dilakukan melalui reaksi esterifikasi menggunakan katalis asam sulfat (2 M) ditambahkan kepada suspensi campuran kitosan dan asam alkanoat pada suhu kamar. Campuran dipanaskan pada suhu 80oC selama 4 jam disertai pengadukan. Asam sulfat yang ditambahkan akan membentuk ion hidrogen sulfit sebagai konter ion dari NH3+, selanjutnya berfungsi untuk memproteksi (sebagai gugus pelindung) N-kitosan. Kemudian pada suhu kamar, tambahkan natrium hidrokarbonat sampai pH 7 (netral)
Reaksi Substitusi Dengan Amina
Ikatan dalam amina
Ikatan dalam suatu amina beranalogi langsung dengan ikatan dalam amonia, suatu atomnitrogen sp3 yang terikat pada tiga atom atau gugus lain (H atau R) dan dengan sepasang elektronmenyendiri dalam orbital sp3 yang tersisa.
Dalam garam amina atau garam amonium kuartener,pasangan elektron menyendiri memembentuk ikatan sigma keempat. Kation beranalogi dengan ion amonium.
Suatu molekul amina dengan tiga gugus berlainan yang terikat pada nitrogen akan bersifat kiral;namin,enantiomer dari sebagian besar senyawa amina tidak dapat diisolasi karena terjadinya inverse yang cepat antara bayangan-bayangan cermin pada temperatur kamar. Inversi itu berlangsung lewat keadaan-transisi datar (nitrogen sp2). Akibatnya ialah piramida nitrogen itu menjentik sehingga dindingdalam menjadi dinding luar, mirip payung yang terhenbus angin kencang. Energi yang diperlukan untuk inversi ini sekitar 6 kkal/mol, kira-kira dua kali energi untuk rotasi mengelilingi ikatan sigma karbon-karbon.
Jika suatu nitrogen amina mempunyai tiga substituen yang berlainan dan pengubahan timbalbalik antara kedua struktur bayangan cermin itu terhalang, maka dapatlah diisolasi sepasang enantiomer. Basa Troger adalah suatu contoh molekul semacam itu. Titian metilena antara kedua nitrogen mencegah pengubahan timbalbalik (inverkonversi) antara banyangan cermin, sehingga basa Troger dapat dipisahkan menjadi sepasang enantiomer.
Kasus lain dimungkinkan adanya enantiomer yang dapat diisolasi ialah pada garam amonium kuterner. Senywa ini secara struktur mirip senywa yang mengandung atom karbon sp3. Jika empat gugus yang berlainan terikat pada nitrogen, ion itu akan bersifat kiral dan garam itu dapat dipisah sebagai enantiomer – enantiomer.
Penggunaan amina dalam sintesis
Sintesis senyawa yang mengandung nitrogen mendapatkan perhatian khusus dari para ahli kimia organik yang berkecimpung dalam farmakologi dan ilmu pngetahuan biologis lainnya, karena banyak biomolekul yang mengandung nirogen. Sebagian besar yang digunakan untuk mensintesis senyawa nitrogen dari amina telah dibahas dalam buku lain.
Banyak reaksi amina adalah hasil serangan nukleofilik oleh elektron menyendiri dari nitrogen amina. Reaksi substitusi suatu amina dengan alkil halida adalah suatu contoh dari amina yang bertindak sebagai suatu nukleofil. Amina dapat juga digunakan sebagai nukleofil dalam reaksi substitusi asil nukleofilik. Jika derivat asam karboksilat merupakan reagensia karbonilnya, maka diperolehamida sebagai produk. Jika reaksi karbonil berupa aldehid atau keton, produknya dalah imina (dari amina primer, RNH2) atau suatu enamina (dari suatu amina sekunder, R2NH).
-NR3+OH-) merupakan suatu teknik sintetik lain. Eliminasi Hofmann dari amonium kuarter hidroksida, lebih berguna sebagai suatu alat analitis dari pada suatu alat sintetik, karena dihasilkan campuran alkena. (juga, suatu reaksi eliminasi alkil halida merupakan jalur yang lebih mudah menuju alkena di laboratorium). Bahkan spektroskopi nmr telah lebih bayak digunakan sebgai suatu alat bantu dalam suatu struktur dari pada eliminasi Hofmann. Di pihak lain,pengubahan suatu arilamina menjadi garam diazonium yang disusul reaksi substitusi, sangat berguna dalam sitesis organik, dan untuk memeriksa tipe senyawa yang mudah diperoleh dari garam arildiazonium.
PERMASALAHAN!!!
1. Amina bersifat basa dan dapat berefleksi secara reversibel.....nah apakah amina selalu berefleksi secara reversibel, dan apa yang di hasilkan jika amina ini tidak berefleksi secara reversibel?
2.bagaimana cara menghilangkan terjadinya inversi pada senyawa amina sehingga senyawa amina ini bisa di isolasi dan apa yang dihasilkan ketika senyawa amina bisa di isolasi?
3. Apakah suatu nitrogen amina harus mempunyai 3 subtituen yang berlawanan saja baru bisa diisolasi dengan sepasang enentiomer? Bagaimana jika nitrogen amina mempunyai 4 subtituen yang berlawanan apa yang akan terjadi?
2.bagaimana cara menghilangkan terjadinya inversi pada senyawa amina sehingga senyawa amina ini bisa di isolasi dan apa yang dihasilkan ketika senyawa amina bisa di isolasi?
3. Apakah suatu nitrogen amina harus mempunyai 3 subtituen yang berlawanan saja baru bisa diisolasi dengan sepasang enentiomer? Bagaimana jika nitrogen amina mempunyai 4 subtituen yang berlawanan apa yang akan terjadi?
- Dapatkan link
- X
- Aplikasi Lainnya










Assallamuaallaikum...
BalasHapusBaik lah saya akan menjawab permasalahan anda no 2 :
Suatu molekul amina dengan tiga gugus berlainan yang terikat pada nitrogen akan bersifat kiral;namin,enantiomer dari sebagian besar senyawa amina tidak dapat diisolasi karena terjadinya inverse yang cepat antara bayangan-bayangan cermin pada temperatur kamar. Inversi itu berlangsung lewat keadaan-transisi datar (nitrogen sp2). Akibatnya ialah piramida nitrogen itu menjentik sehingga dindingdalam menjadi dinding luar, mirip payung yang terhenbus angin kencang. Energi yang diperlukan untuk inversi ini sekitar 6 kkal/mol, kira-kira dua kali energi untuk rotasi mengelilingi ikatan sigma karbon-karbon.
Jika suatu nitrogen amina mempunyai tiga substituen yang berlainan dan pengubahan timbalbalik antara kedua struktur bayangan cermin itu terhalang, maka dapatlah diisolasi sepasang enantiomer. Basa Troger adalah suatu contoh molekul semacam itu. Titian metilena antara kedua nitrogen mencegah pengubahan timbalbalik (inverkonversi) antara banyangan cermin, sehingga basa Troger dapat dipisahkan menjadi sepasang enantiomer.
Kasus lain dimungkinkan adanya enantiomer yang dapat diisolasi ialah pada garam amonium kuterner. Senywa ini secara struktur mirip senywa yang mengandung atom karbon sp3. Jika empat gugus yang berlainan terikat pada nitrogen, ion itu akan bersifat kiral dan garam itu dapat dipisah sebagai enantiomer – enantiomer.
Saya akan menjawab permasalahan nomor 3 yang ada di link ini https://www.google.com/url?sa=t&source=web&rct=j&url=http://dwi.blog.unsoed.ac.id/files/2013/04/KOII-8-SENYAWA-AMINA.pdf&ved=2ahUKEwiU8sumlMLdAhUMRY8KHdiJBtkQFjAAegQIAhAB&usg=AOvVaw1QyfR1J_6aG0wm1twbaTXp
BalasHapusSaya akan mencoba menjawab permasalahan anda yg ke-2 Jika terdapat substituen yang tidak terikat pada gugus –NH, maka nama substituen ditulis lebih dulu.
BalasHapusTetapi, jika substituen terikat pada gugus –NH dan substituen tersebut sejenis dengan gugus alkil yang terikat pada gugus –NH, maka penulisnya diawali dengan N,posisi substituen.
Untuk amina primer:
Perhatikan angka di depan nama substituen yang menunjukkan atom karbon yang mengikat substituen tersebut dan tarik garis dari atom karbon tersebut.
Untuk amina sekunder:Untuk substituen, perhatikan angka setelah huruf N atau angka terdepan pada nama senyawa. Jika terdapat angka setelah huruf N, maka struktur substituen sejenis dengan struktur gugus alkil yang terikat pada gugus –NH.
Untuk amina tersier:Jika terdapat nama substituen (di depan huruf N), perhatikan angka di depan nama substituen yang menunjukkan posisi atom karbon yang terikat dengan substituen tersebut. Tarik garis dari atom karbon tersebut.
No2. Jika suatu nitrogen amina mempunyai tiga substituen yang berlainan dan pengubahan timbalbalik antara kedua struktur bayangan cermin itu terhalang, maka dapatlah diisolasi sepasang enantiomer. Basa Troger adalah suatu contoh molekul semacam itu. Titian metilena antara kedua nitrogen mencegah pengubahan timbalbalik (inverkonversi) antara banyangan cermin, sehingga basa Troger dapat dipisahkan menjadi sepasang enantiomer.
BalasHapusKasus lain dimungkinkan adanya enantiomer yang dapat diisolasi ialah pada garam amonium kuterner. Senywa ini secara struktur mirip senywa yang mengandung atom karbon sp3. Jika empat gugus yang berlainan terikat pada nitrogen, ion itu akan bersifat kiral dan garam itu dapat dipisah sebagai enantiomer – enantiomer.
Tetapi, jika substituen terikat pada gugus –NH dan substituen tersebut sejenis dengan gugus alkil yang terikat pada gugus –NH, maka penulisnya diawali dengan N,posisi substituen.
Untuk amina primer:
Perhatikan angka di depan nama substituen yang menunjukkan atom karbon yang mengikat substituen tersebut dan tarik garis dari atom karbon tersebut.
Untuk amina sekunder:Untuk substituen, perhatikan angka setelah huruf N atau angka terdepan pada nama senyawa. Jika terdapat angka setelah huruf N, maka struktur substituen sejenis dengan struktur gugus alkil yang terikat pada gugus –NH.
Untuk amina tersier:Jika terdapat nama substituen (di depan huruf N), perhatikan angka di depan nama substituen yang menunjukkan posisi atom karbon yang terikat dengan substituen tersebut. Tarik garis dari atom karbon tersebut.
Jawaban untuk permasalahan no 3.
BalasHapus3 subtituen yg beralawanan maksudnya , nitrogen pada amina hanya memiliki 3 tangan, jadi maksimal atom yg dapat diikatnya adalah 3, tidak bisa 4 atau 5, karena nitrogen kekurangan 3 elektron untuk mencapai kestabilan, terima kasih
Titian metilena antara kedua nitrogen mencegah pengubahan timbalbalik (inverkonversi) antara banyangan cermin, sehingga basa Troger dapat dipisahkan menjadi sepasang enantiomer.
BalasHapusKasus lain dimungkinkan adanya enantiomer yang dapat diisolasi ialah pada garam amonium kuterner. Senywa ini secara struktur mirip senywa yang mengandung atom karbon sp3. Jika empat gugus yang berlainan terikat pada nitrogen, ion itu akan bersifat kiral dan garam itu dapat dipisah sebagai enantiomer – enantiomer.
Saya akan mencoba menjawab permasalahan Anda yg ke-2:
BalasHapusSifat-sifat struktural yang sama yang mempengaruhi kuat asam relatif dari asam karboksilat dan fenol juga mempengaruhi kuat basa relatif dari amina
Jika amina bebas terstabilkan relatif terhadap kationnya, maka maka amina itu merupakan basa yang lebih lemah
Jika kation itu terstabilkan relatif terhadap amina bebasnya, maka amina itu adalah basa yang lebih kuat.
Permasalaha 2 adanya enantiomer yang dapat diisolasi ialah pada garam amonium kuterner. Senywa ini secara struktur mirip senywa yang mengandung atom karbon sp3. Jika empat gugus yang berlainan terikat pada nitrogen, ion itu akan bersifat kiral dan garam itu dapat dipisah sebagai enantiomer – enantiomer.
BalasHapussaya akan menjawab permasalahan anda no 2 :
BalasHapusSuatu molekul amina dengan tiga gugus berlainan yang terikat pada nitrogen akan bersifat kiral;namin,enantiomer dari sebagian besar senyawa amina tidak dapat diisolasi karena terjadinya inverse yang cepat antara bayangan-bayangan cermin pada temperatur kamar. Inversi itu berlangsung lewat keadaan-transisi datar (nitrogen sp2). Akibatnya ialah piramida nitrogen itu menjentik sehingga dindingdalam menjadi dinding luar, mirip payung yang terhenbus angin kencang. Energi yang diperlukan untuk inversi ini sekitar 6 kkal/mol, kira-kira dua kali energi untuk rotasi mengelilingi ikatan sigma karbon-karbon.
Saya akan mencoba menjawab permasalahan Anda yg ke-2:
BalasHapusSifat-sifat struktural yang sama yang mempengaruhi kuat asam relatif dari asam karboksilat dan fenol juga mempengaruhi kuat basa relatif dari amina
Jika amina bebas terstabilkan relatif terhadap kationnya, maka maka amina itu merupakan basa yang lebih lemah
Jika kation itu terstabilkan relatif terhadap amina bebasnya, maka amina itu adalah basa yang lebih kuat.
saya akan menjawab permasalahan anda no 2 :
BalasHapusSuatu molekul amina dengan tiga gugus berlainan yang terikat pada nitrogen akan bersifat kiral;namin,enantiomer dari sebagian besar senyawa amina tidak dapat diisolasi karena terjadinya inverse yang cepat antara bayangan-bayangan cermin pada temperatur kamar. Inversi itu berlangsung lewat keadaan-transisi datar (nitrogen sp2). Akibatnya ialah piramida nitrogen itu menjentik sehingga dindingdalam menjadi dinding luar, mirip payung yang terhenbus angin kencang. Energi yang diperlukan untuk inversi ini sekitar 6 kkal/mol, kira-kira dua kali energi untuk rotasi mengelilingi ikatan sigma karbon-karbon.
Baiklah saya akan mencoba menjawaban untuk permasalahan nomor tiga yaitu 3 subtituen yg beralawanan maksudnya , nitrogen pada amina hanya memiliki 3 tangan, jadi maksimal atom yg dapat diikatnya adalah 3, tidak bisa 4 atau 5, karena nitrogen kekurangan 3 elektron untuk mencapai kestabilan,
BalasHapussaya akan menjawab permasalahan anda no 2 :
BalasHapusSuatu molekul amina dengan tiga gugus berlainan yang terikat pada nitrogen akan bersifat kiral;namin,enantiomer dari sebagian besar senyawa amina tidak dapat diisolasi karena terjadinya inverse yang cepat antara bayangan-bayangan cermin pada temperatur kamar. Inversi itu berlangsung lewat keadaan-transisi datar (nitrogen sp2). Akibatnya ialah piramida nitrogen itu menjentik sehingga dindingdalam menjadi dinding luar, mirip payung yang terhenbus angin kencang. Energi yang diperlukan untuk inversi ini sekitar 6 kkal/mol, kira-kira dua kali energi untuk rotasi mengelilingi ikatan sigma karbon-karbon.